Российские ученые продемонстрировали,
что прием препаратов из биомассы культур клеток японского женьшеня, диоскореи
дельтовидной и якорцев стелющихся замедляет увеличение веса у крыс с ожирением.
Выращиваемые в биореакторах клетки этих лекарственных растений синтезируют
биологически активные вещества, способные нормализовать нарушенный болезнью
обмен веществ. Полученные на их основе фитопрепараты могут стать эффективной и
безопасной альтернативой синтетическим лекарствам против ожирения, для многих
из которых присущ ряд противопоказаний и побочных эффектов. Результаты
работы, поддержанной грантом
Российского научного фонда (РНФ), опубликованы в
журнале Nutrients.

Колбы: исходные культуры клеток
диоскореи дельтовидной, женьшеня японского и якорцев стелющихся, поддерживаемые
во Всероссийской коллекции культур клеток высших растений ИФР РАН. Нижний ряд:
сухая биомасса тех же культур, выращенных в биореакторах.
Ожирение – чрезмерное отложение жировой ткани, как
правило, связанное с нарушенным обменом веществ и представляющее опасность для
здоровья и даже жизни. Патологии метаболизма могут быть вызваны как
разнообразными заболеваниями, так и малоактивным образом жизни вкупе с
высококалорийным питанием. Ожирение встречается примерно у каждого
третьего россиянина и каждого десятого человека на планете.
Ожирение является одним из основных факторов риска, связанных с развитием
астмы, диабета второго типа, некоторых видов рака, сердечно-сосудистых
заболеваний, нарушений опорно-двигательного аппарата, осложнений после острых
инфекционных заболеваний, в том числе SARS-CoV-2. Поэтому неудивительно, что
достаточно часто возникают проблемы с подбором синтетических препаратов для
лечения ожирения, которые сочетались бы с другими лекарствами и были бы
безопасны с учетом имеющихся патологических состояний.
В новой работе сотрудники Института
физиологии растений имени К.А. Тимирязева Российской академии наук (Москва)
совместно с коллегами из Санкт-Петербургского
государственного химико-фармацевтического университета (Санкт-Петербург)
обратили внимание на природные вещества, которые синтезируют растения. Обычно
это смесь соединений, которые оказывают комплексный эффект, однако в
дикорастущих растениях сложно контролировать содержание и состав целевых
молекул. Это может быть чревато как недостаточным терапевтическим эффектом от
нужных веществ, так и отравлением из-за наличия их токсичных форм.
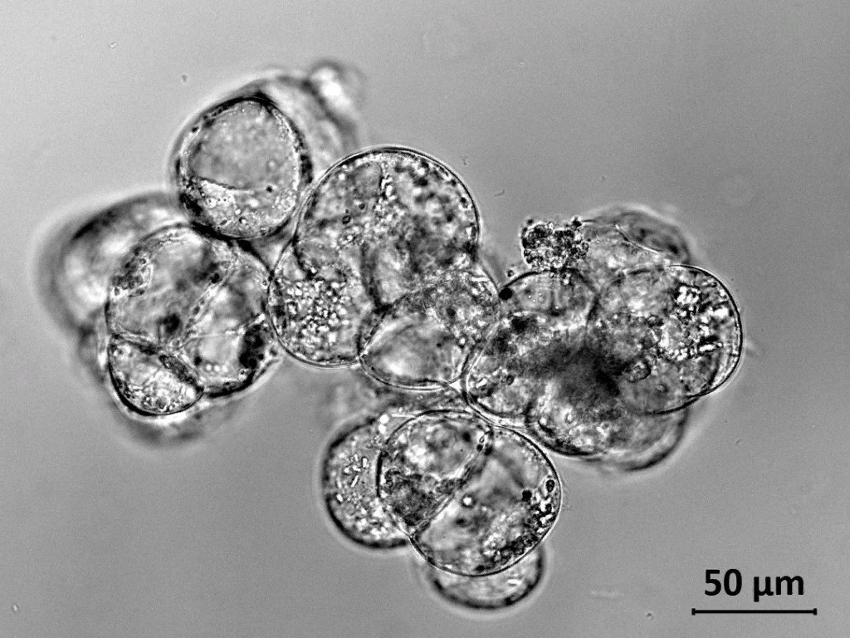
Клетки суспензионной культуры женьшеня
японского под микроскопом. Источник: ИФР РАН.
Авторы пошли по пути
использования биотехнологических подходов: получили и вырастили клетки трех
лекарственных растений – японского женьшеня, диоскореи дельтовидной и якорцев
стелющихся – в специальных биореакторах. Предыдущие исследования показали,
что экстракты этих культур оказывают значимое положительное воздействие на
организм лабораторных животных с нарушением углеводного обмена за счет
активности тритерпеновых и стероидных гликозидов. Полученные из диких растений
культуры клеток вырабатывали определенное количество известных биологически
активных веществ, а промышленные установки обеспечили им для этого оптимальные
условия: подбирая состав питательной среды и условия выращивания клеток,
удается четко контролировать и даже специально изменять спектр и содержание
целевых соединений.
Экстракты из выращенной биомассы ученые использовали как биодобавку для крыс с
уже развившимся ожирением – животным при этом продолжали давать очень
калорийный корм. На протяжении трех месяцев авторы сравнивали состояние
грызунов на такой диете с контрольными «полными» животными на калорийном и
стандартном корме, а также с теми, которые находились на избыточном кормлении,
но получали инъекции популярного синтетического препарата от ожирения
(лираглутида). С помощью биоимпедансной спектроскопии (основана на различном
сопротивлении тканей разной структуры электрическому току) ученые оценивали
долю жира в массе тела крыс, баланс внутри- и внеклеточной жидкости; также
проводили биохимический и общий анализ крови.
Результаты показали, что наибольший эффект дал фитопрепарат диоскореи
дельтовидной – в некоторых исследованиях он превосходил даже лираглутид. Так,
спустя три месяца лечения препаратом набор веса у крыс замедлился, и процент
жировой массы составил в среднем 28 %, тогда как у их сородичей на калорийном и
стандартном корме – 41,5 и 36 % соответственно, а у животных, получавших
лираглутид, – 36 %. В ходе исследования все три фитопрепарата также вызывали
снижение уровней глюкозы и холестерина в крови, причем их действие оказалось
сравнимым с синтетическим лираглутидом.
На следующем этапе авторы решили проверить, насколько безопасен самый
эффективный из изученных препаратов – на основе диоскореи дельтовидной – для
потомства животных. Все получавшие его крысы остались плодовитыми, хотя и
приносили детенышей на 12 % меньше, чем контрольные крысы без фитопрепаратов.
Ни в одной группе не было зафиксировано смертей или аномального развития среди
потомства. Малыши, чьи родители получали препарат диоскореи, набирали массу
интенсивнее – прибавка составила 49 % против 36 % в группе контроля. Также они имели
более сильную антиоксидантную защиту, которая не дает разрушать клетки слишком
агрессивным свободным радикалам, образующимся в норме и при воспалительных
реакциях.
«Эти результаты говорят
в пользу того, что фитопрепарат можно потенциально использовать и для лечения
ожирения у женщин детородного возраста. Однако о применении на людях говорить
пока рано – наше исследование можно назвать первичным скринингом биологической
активности биомассы клеток диоскореи дельтовидной, якорцев стелющихся и
женьшеня японского. В дальнейшем мы хотим провести эксперименты на моделях
других типов ожирения, например, вызванного диабетом. Они помогут открыть новые
возможности в лечении ожирения и связанных с ним осложнений», – рассказывает
руководитель проекта, поддержанного грантом РНФ, заведующий отделом биологии
клетки и биотехнологии ИФР РАН, доктор биологических наук, профессор Александр
Носов.

630-литровый биореактор для выращивания
культур клеток высших растений, Опытный биотехнологический комплекс ИФР РАН.
Источник: ИФР РАН.
Лекарственные растения часто используются для
терапии ожирения, но уникальным в исследованиях ученых является именно наработка
растительной клеточной биомассы в биореакторах, то есть в полностью
контролируемых, стерильных условиях. Технологии, разработанные в ИФР РАН,
позволяют в течение всего года получать нужные количества продукта с заданным
стабильным качеством.
«Это значит, что в будущем мы сможем
предложить производителям лекарств и пищевых добавок экологически чистый,
возобновляемый источник лекарственного растительного сырья без необходимости
сбора растений в дикой природе или выращивания на плантациях. Учитывая, что
многие лекарственные растения являются редкими и исчезающими или в принципе не
растут на территории нашей страны, такой подход позволит более полно
использовать их потенциал без вреда для экологии и с пользой для человека», –
подводит итог Александр Носов.
В работе также приняли участие исследователи Московского государственного
университета имени М. В. Ломоносова (Москва) и Всероссийского научно-исследовательского
института мясной промышленности имени В. М. Горбатова (Москва).
Источник: пресс-служба РНФ.