http://93.174.130.82/news/shownews.aspx?id=b5b274c1-1ccb-4bf7-8938-a2750a341388&print=1
© 2025 Российская академия наук
Сотрудники Красноярского научного центра СО РАН разработали микросферы, которые могут применяться для радиационной терапии онкологических заболеваний печени. Основой для них стали полые алюмосиликатные микросферы (ценосферы) из летучих зол, получаемых в результате сжигания угля. Результаты исследования опубликованы в «Журнале Сибирского федерального университета. Химия» и журнале Materials.
Поиск способов диагностики и терапии злокачественных опухолей — одна из наиболее актуальных проблем медицины. Большие перспективы в этой области имеет адресная доставка радионуклидов к опухоли, в частности, терапия, основанная на введении микросфер, содержащих радионуклидный препарат, в сосуды, питающие опухоль. Сейчас для этого применяются наноструктурированные стеклянные микросферы на основе иттрия-90, которые, однако, имеют высокую стоимость.
Учёные ФИЦ «Красноярский научный центр СО РАН» получили алюмосиликатные микросферы на основе ценосфер с изотопом лютеция-176. Низкая токсичность ценосфер делает возможным их применение в биохимии и медицине. Эти материалы можно будет использовать в качестве предшественника микроисточника бета-излучения для проведения брахитерапии — метода лечения рака печени за счет радиоактивного облучения. Это позволит снизить стоимость микросфер, поскольку полые алюмосиликатные микросферы выделяются из летучих зол, получаемых в результате сжигания угля.
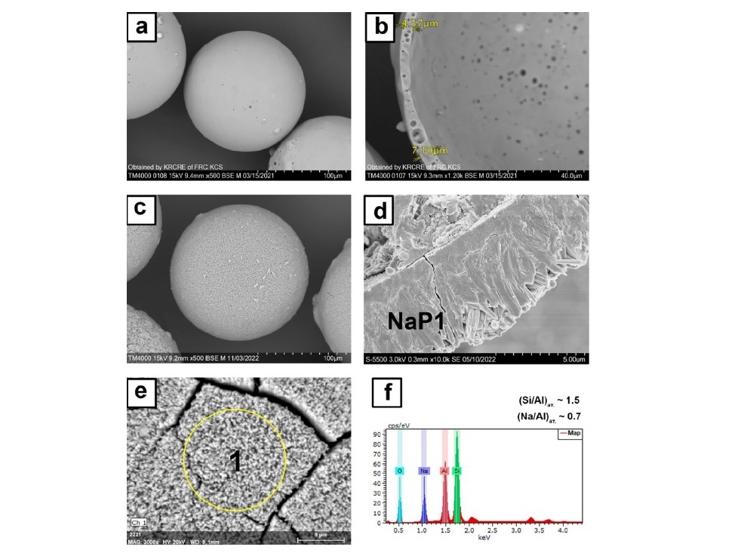
РЭМ снимки исходных ценосфер (а), скола стенки ценосфер (b), глобулы (с) и сечения стенки (d) цеолитизированных микросфер; EDX спектр (e) участка цеолитного покрытия (f, e‑1)
Исследователи предложили оригинальную методику для включения ионов лютеция в алюмосиликатный материал ценосфер. Новый подход включает несколько этапов. Первый — химическая модификация ценосфер путем превращения алюмосиликатного стекла в цеолиты. Второй — концентрирование стабильного изотопа лютеция-176 путем ионного обмена в пористой структуре цеолита. Последний — третий — этап — термическое воздействие и превращение лютеция в малорастворимые формы. В результате получаются алюмосиликатные стеклокомпозитные микросферы с внедренной малорастворимой формой лютеция-176. Радиоактивными такие микросферы становятся после облучения в ядерном реакторе непосредственно перед проведением радиотерапии.
Учёные также определили скорость выщелачивания лютеция. В медицине скорость выщелачивания используется для изучения взаимодействия лекарственных препаратов с тканями организма, а также для оценки токсичности материалов. Эксперименты проводились в растворе хлорида натрия, имитирующем состав крови. Полученные микросферы характеризовались низкой скоростью выхода лютеция, что говорит о безопасности данных материалов для использования в медицине.
«Нами были получены микросферы с внедренным лютецием-176 в качестве предшественника микросферического источника бета-излучения. Их можно применять для селективной радиационной терапии раковых опухолей печени. Эти частицы нетоксичны и безопасны, поскольку изотоп лютеция располагается в глубоких слоях оболочки микросфер, соответственно, его прямой контакт с живыми тканями отсутствует. Актуальная задача дальнейшего исследования — получение микросфер с оптимальными физическими параметрами, например, размером 20–40 микрометров, эффективной плотностью 1,1–1,2 г/см³ и минимальным содержанием нежелательных примесей»,— рассказала кандидат химических наук научный сотрудник Института химии и химической технологии (ИХХТ) СО РАН Екатерина Кутихина.
Исследование выполнено при поддержке Российского научного фонда и Красноярского краевого фонда науки. Руководитель проекта — Татьяна Верещагина, доктор химических наук, ведущий научный сотрудник Института химии и химической технологии СО РАН.
Источник: Служба научных коммуникаций ФИЦ «Красноярский научный центр СО РАН».