Сотрудники факультета фундаментальной медицины МГУ в составе международной исследовательской группы впервые провели комплексную оценку воздействия злокачественных опухолей на прилегающие к ним нормальные ткани. Именно эти ткани чаще всего используются в онкологии в качестве контрольных образцов при анализе новообразований, и до настоящего времени корректность их применения в таких целях не ставилась под сомнение. В ходе данной работы специалисты доказали, что несмотря на визуальную «нормальность» тканей, прилегающих к опухоли, такое соседство не проходит бесследно.
Оно влечет за собой целый ряд молекулярных изменений на уровне экспрессии генов, которые удалось обнаружить с помощью сравнения с образцами здоровых тканей. Результаты работы позволяют по-новому взглянуть на современные подходы к анализу опухолей и проблему выбора подходящего контроля для проведения онкологических исследований. Они значимы как для фундаментальной науки, так и для прикладных целей, включая область персонализированной медицины. Работа опубликована в Computational and Structural Biotechnology Journal.
Отличительной чертой опухолевых клеток по сравнению с нормальными является нарушение регуляции экспрессии генов. Эта ключевая особенность, выраженная в четырех словах, подразумевает под собой огромный комплекс всевозможных изменений в работе молекулярных механизмов геномного контроля и является предметом многочисленных исследований учёных. Сравнительная оценка экспрессии генов в опухолевых и здоровых клетках помогает выявить характерные для патологического процесса нарушения и широко используется как для изучения онкологических заболеваний, так и в медицинской практике. Для этого применяют современные подходы, например, транскриптомный и протеомный анализ.
«Чем больше мы узнаем о различиях в регуляции молекулярных процессов в здоровых и опухолевых клетках, тем совершеннее становятся стратегии диагностики и терапии онкологических заболеваний. Уже сегодня эти данные успешно используются в персонализированной медицине для выбора схемы лечения. Однако, чтобы быть уверенными, что молекулярные нарушения связаны именно с патологическим процессом, необходимо, чтобы контрольные образцы не давали “ложных показаний”. Именно этот вопрос мы всесторонне изучили в данном исследовании, обозначив проблемы современных подходов и пути их решения», — пояснил доцент факультета фундаментальной медицины МГУ Нуршат Гайфуллин.
На сегодняшний день в онкологических исследованиях для оценки экспрессии генов используют два типа контроля — здоровые ткани или же морфологически нормальные ткани, прилегающие к опухоли. Второй вариант применяется наиболее часто. Это обусловлено тем, что доступ к здоровым человеческим тканям возможен только после посмертного вскрытия (аутопсии). По этой причине в большинстве экспериментов используются ткани, расположенные по соседству с очагом опухоли. До настоящего времени вопрос о том, насколько приемлемо их использование для этих целей, не был изучен детально. Специалисты факультета фундаментальной медицины МГУ совместно с коллегами заострили внимание на этой проблеме. Они впервые оценили характер и масштаб воздействия новообразований на прилегающие к ним ткани и показали, что их «нормальность» весьма условна.
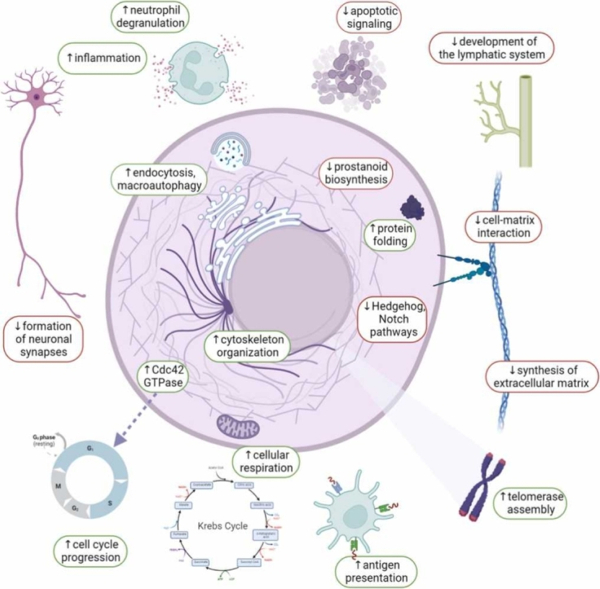
В ходе работы специалисты оценили уровень экспрессии генов для трех групп образцов, а именно: для здоровых тканей, полученных при помощи аутопсии, нормальных тканей, прилегающих к очагу опухоли, и самих опухолей. Они обнаружили целый комплекс молекулярных различий между двумя типами тканей, используемых в качестве контроля. Прилегающие к опухоли ткани отличались от здоровых рядом характеристик, связанных с активацией иммунных клеток, внутриклеточным транспортом, клеточным дыханием, реорганизацией внеклеточного матрикса. Ученые пришли к выводу, что эти различия вызваны именно соседством с злокачественной опухолью, поскольку между новообразованиями и прилегающими тканями были зафиксированы общие нарушения в регуляции молекулярных процессов. Чтобы убедиться в достоверности обнаруженных тенденций, учёные проанализировали в общей сложности более 5 000 профилей генной экспрессии.
«Благодаря нашему исследованию масштаб воздействия опухолей на прилегающие ткани стал очевиден. Разумеется, этот феномен не может не сказываться на точности интерпретации данных генной экспрессии, которая очень важна для персонализированной медицины. Мы обнаружили в прилегающих к опухоли тканях отклонения в работе 69 генов, имеющих особую значимость при выборе таргетной терапии. Правильная оценка их функционирования является определяющей для назначения по меньшей мере 52 противоопухолевых препаратов», — прокомментировал Нуршат Гайфуллин. По словам исследователя, полученные в ходе исследования данные помогут избежать ошибок при выборе индивидуальной схемы лечения в случае, когда для диагностики в качестве контроля используются прилегающие к опухоли ткани.
Помимо основного вектора исследования, учёные также коснулись вопроса использования в качестве контроля здоровых тканей, полученных при помощи аутопсии. Они подчеркнули, что такая альтернатива не так уж «идеальна», как казалось прежде. Здоровые ткани тоже могут стать источником «ложных показаний», причем в зависимости от времени хранения после аутопсии в них обнаруживается все больше отклонений в работе молекулярных механизмов. Любопытно, что масштаб этих изменений зависит от типа ткани. Например, в ходе испытаний на животных специалисты выяснили, что уже через сутки после проведения аутопсии в тканях легкого обнаруживаются отклонения в экспрессии более 1 000 генов.
Изученный в данной работе феномен помимо фундаментальной значимости напрямую затрагивает актуальные проблемы медицинской практики. Проведённое исследование акцентирует внимание на проблемах, которые возникают при использовании двух типов контроля, применяемых в онкологии для анализа новообразований. Предложенные учеными рекомендации для учета молекулярных изменений в контрольных образцах позволят точнее интерпретировать результаты транскриптомного анализа.
Источник: МГУ.