Антибиотик ванкомицин в защитном покрытии магниевого имплантата предотвратит инфекции при протезировании костей
11.07.2024
Исследователи из
нескольких научных учреждений Владивостока и Москвы сформировали на образцах
магниевого сплава кальций-фосфатное покрытие для костных имплантатов,
содержащее антибиотик ванкомицин. Покрытие повысило коррозионную устойчивость
сплава в два раза. При этом оно обладало выраженным антибактериальным
действием, не подавляло рост человеческих клеток и предотвращало воспаление
после имплантации образцов в ткани животных.
Таким образом,
полученные изделия повысят успешность и безопасность протезирования костей.
Результаты исследования, поддержанного грантами Российского научного фонда (РНФ), опубликованы в Journal of Magnesium and Alloys.
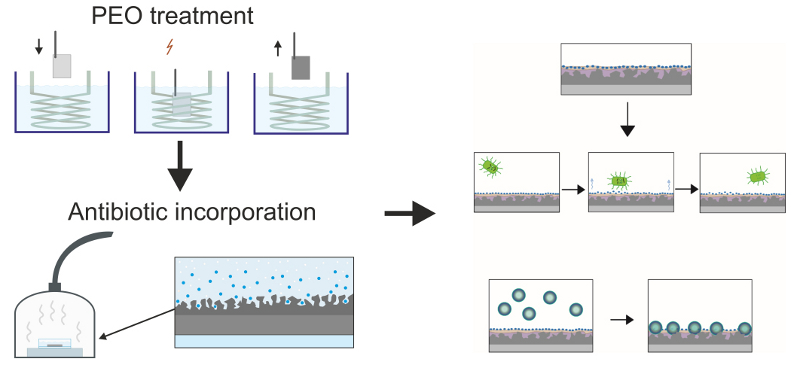
Схема формирования и
работы покрытия
Костные имплантаты
обычно изготавливают из биоинертных металлов и сплавов, например титана. Такие
соединения не растворяются в организме и в ряде случаев требуют удаления после
восстановления костей. В отличие от них, магний и его сплавы удалять не нужно,
так как они безопасно разлагаются и рассасываются в организме. Однако магниевые
сплавы обладают низкой коррозионной стойкостью, то есть со временем они
разрушаются, а продукты коррозии могут вызывать воспалительные процессы в
организме. Чтобы предотвратить коррозию магниевых сплавов, но при этом
сохранить их способность к разложению, учёные разрабатывают биосовместимые
защитные покрытия. Однако на данный момент многие из таких покрытий плохо
связываются с основой имплантата, расслаиваются и трескаются.
Исследователи из
Института химии ДВО РАН (Владивосток) с коллегами изучили,
как покрытие из фосфатов кальция влияет на коррозионную стойкость и
биосовместимость имплантатов из сплава на основе магния. Выбранное покрытие
состояло из элементов, присутствующих и усваивающихся в организме человека.
Чтобы сформировать
покрытие, авторы поместили магниевые образцы в раствор, содержащий соединения
кальция и фосфора, и пропустили через него электрический ток. В результате на
сплаве был сформирован гидроксиапатит — основной минеральный компонент костной ткани.
Затем в образцы с покрытием внедрили антибиотик ванкомицин, который
используется для борьбы с инфекциями, возникающими после имплантации. Авторы
рассчитывали, что такая обработка антибиотиком снизит вероятность развития
инфекций после помещения имплантатов в живой организм. Толщина покрытия не
превышала 0,1 миллиметра, при этом кальций и фосфор распределились по нему
равномерно. На поверхности образца сформировались поры разного диаметра,
глубины и формы. Такая поверхность будет способствовать хорошей приживаемости
имплантата за счёт прорастания соединительной ткани человека в поры покрытия.

Изображение полученных
покрытий без ванкомицина (PEO, a) и с ванкомицином (PEO-V, b) и карты
распределения элементов, входящих в состав покрытия
Также химики показали,
что покрытие, содержащее гидроксиапатит, в два раза повысило коррозионную
стойкость изделий. Таким образом, оно будет предотвращать преждевременное
разрушение имплантата и неконтролируемое высвобождение ионов магния в организм.
Затем исследователи
изучили антибактериальные свойства сформированных магниевых образцов с
покрытием. Для этого авторы поместили образцы в чашки Петри с культурой клеток
золотистого стафилококка (Staphylococcus aureus) — бактерий, образующих
биопленки на медицинских имплантатах и в прилегающих тканях и вызывающих
воспаление. Внедрение в покрытие антибиотика позволило эффективно уничтожать
бактерии.
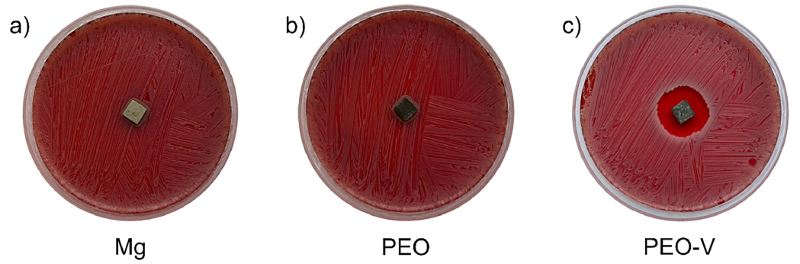
Результаты
антибактериального теста. Изображения чашек Петри с культурой золотистого
стафилококка, инкубированной в присутствии различных типов образцов: без
покрытия (Mg, а), с покрытиями без (PEO, b) и с (PEO-V, c) внедрённым
ванкомицином
Учёные установили, что
антибиотик интенсивно выделялся из пор покрытия в первые четыре дня
эксперимента. Так как имплантат-ассоциированные инфекции с наибольшей
вероятностью возникают именно в первые дни после операции, выделение
антибиотика будет активно подавлять их развитие. С седьмых суток концентрация
ванкомицина в моделируемой жидкости организма почти не менялась, а к 28 суткам
антибиотик полностью высвободился из пор покрытия. Таким образом, спустя неделю
после имплантации оставшиеся низкие концентрации препарата будут предотвращать
возвращение инфекций и образование бактериальной биопленки, но не будут мешать
прикреплению клеток человека к поверхности имплантата.
Кроме того, авторы
проверили, не токсично ли покрытие. Для этого образцы смешали с клетками
пигментного эпителия сетчатки человека — одной из самых популярных клеточных
культур, используемой для тестирования совместимости веществ с человеческими
клетками. Образцы с покрытием, содержащим антибиотик, практически не подавляли
клеточный рост, в то время как сплав без покрытия подавлял рост клеток на 58%,
что ставит под сомнение безопасность использования чистых магниевых сплавов в
качестве имплантатов.
Также химики проверили,
будет ли имплантация образцов в область позвоночника самцов крыс вызывать
воспалительные реакции. У животных с имплантированными образцами без покрытия
наблюдалась местная воспалительная реакция: постепенное образование продуктов
коррозии привело к появлению гнойных капсул вокруг образцов. Напротив, в местах
имплантации образцов с кальций-фосфатным покрытием не было обнаружено признаков
воспаления. Биохимические показатели крови, анализ мочи, анализ свёртываемости
крови у экспериментальных животных после имплантации показали, что
сформированные покрытия не вызывают системного воспаления в организме и не
имеют токсического эффекта.
«Разработанное покрытие
позволяет нивелировать негативные свойства магниевых сплавов, расширяя
возможности их использования в имплантологии. Наши дальнейшие исследования
будут направлены на улучшение полученных материалов, создание гибридных слоев,
содержащих противоопухолевые и подавляющие разрушение костной ткани вещества»,
— рассказывает руководитель проекта, поддержанного грантом РНФ, Константинэ
Надараиа, кандидат химических наук, старший научный сотрудник Института химии
ДВО РАН.

Также в исследовании
приняли участие ученые из Дальневосточного федерального университета (Владивосток),
Национального научного центра морской биологии им/ А.В. Жирмунского ДВО РАН (Владивосток),
Краевого клинического кожно- венерологического диспансера (Владивосток) и НМИЦ
«Лечебно-реабилитационный центр» (Москва).
Источник: РНФ.