http://93.174.130.82/news/shownews.aspx?id=25393d74-e5f4-44dd-8ea5-cb9df5422def&print=1
© 2025 Российская академия наук
Исследователи из Института органического синтеза им. И.Я. Постовского УрО РАН
(Екатеринбург) и ФИЦ проблем химической физики и медицинской химии РАН (Черноголовка) нашли условия для
введения аминоалкиленового спейсера в молекулу антихолинэстеразного препарата амиридина. Это открыло для
химиков-органиков возможности для получения на основе амиридина конъюгатов нового типа.
Созданные учёными конъюгаты амиридина и производных салициловой кислоты
оказались эффективными мультитаргетными лекарственными кандидатами для терапии болезни Альцгеймера.
Исследование опубликовано в журнале Archiv der
Pharmazie.
Деменцию и её самую тяжёлую разновидность, болезнь Альцгеймера, не зря
называют главной пандемией XXI века. Уже сейчас от неё страдает 52 миллиона человек во всем мире, а прогноз
на 2050 год составляет огромные 150 миллионов человек. Используемые в настоящее время для лечения БА
лекарственные препараты являются только симптоматическими средствами и не могут замедлить развитие
собственно нейродегенеративного процесса.
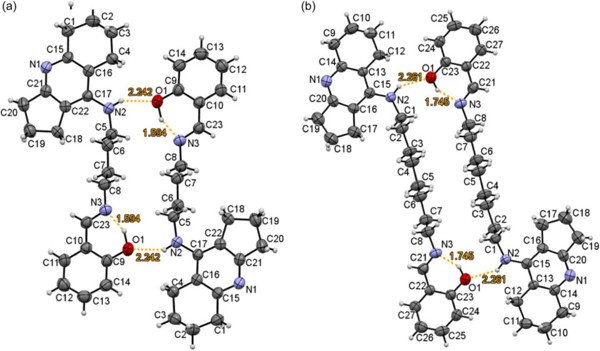
Структура некоторых коньюгатов
Первоначально считалось, что первопричина заболевания — накопление
бета-амилоида в нейронах, и именно на неё были направлены силы всех нейрофармакологов. Однако все препараты,
построенные на этой гипотезе, провалились в клинических испытаниях, а не так давно и к самой научной статье, на которой
базировалась эта гипотеза, появились серьёзные вопросы и публикация была отозвана.
Сейчас болезнь Альцгеймера считается заболеванием с многофакторной
этиологией. Патогенетические факторы заболевания включают нарушение работы нейромедиаторных систем,
агрегацию β-амилоидных и тау-белков, дисбаланс окислительно-восстановительных систем и нарушение регуляции
гомеостаза ионов металлов в нервной системе. Поэтому одной из актуальных стратегий в медицинской химии стало
создания коньюгатов: связанных химическими мостиками мультитаргетных молекул, направленных на несколько
мишеней, вовлеченных в патогенез заболевания.
Среди таких конъюгатов активно рассматриваются вещества на основе ингибиторов
известных холинэстераз, которые через спейсер (химический мостик) связываются с другими фармакофорами,
которые должны обеспечить нейропротекторные и некоторые другие свойства получившейся молекулы.
В новой работе сотрудники Института органического синтеза им. И.Я.
Постовского УрО РАН и ФИЦ Проблем химической физики и медицинской химии РАН сумели связать полиметиленовыми
мостиками молекулу амиридина, которая служит ингибитором ацелилхолинэстераз и производные салициловой
кислоты.
Синтезированные коньюгаты обладали широким спектром фармакологической
активности: они оказались высокоэффективными и обратимыми ингибиторами ацетилхолинэстеразы и
бутирилхолинэстеразы (ферментов, регулирующих проведение нервного импульса в холинергиеских синапсах),
обладали радикал-связывающей активностью (антиоксидантное действие), связыванием катионов меди, цинка и
железа, а главное — эти препараты блокировали агрегацию бета-амилоида в бляшки, как катализируемую
ацетилхолинэстеразой, так и самоагрегацию.
Эксперименты показали хорошее согласование реальных свойств синтезированных
соединений с результатами молекулярного докинга в холинэстеразы и β-амилоид и квантово-химическими расчётами
их антиоксидантной активности. Авторы работы нашли и соединение-лидер, которое обладает самым
перспективным набором свойств и при этом весьма благоприятным ADMET-профилем (важный показатель
фармакологических свойств препарата: Absorption, Distribution, Metabolism, Excretion, and Toxicity —
всасывание, распределение, метаболизм, выведение и токсичность).
Таким образом, на основе отечественного препарата амиридина впервые получены
конъюгаты с широким спектром биологической активности и благоприятным ADMET профилем, которые могут служить
основой для разработки инновационных мультитаргетных препаратов терапии болезни Альцгеймера.
Текст: Алексей Паевский. Источник: «Нейроновости».