Показана перспективность использования частиц наноструктурированного кремния в методах лечения онкологических болезней электромагнитным излучением.
15.08.2019
В настоящее время интенсивно изучаются возможности
лечения онкологических болезней электромагнитным излучением. Действующим
агентом в этих методах являются вещества, предварительно помещаемые в ткань и
интенсивно поглощающие электромагнитное излучение. Это вызывает нагрев ткани и
соответственно гибель клеток в зоне повышенной температуры.
Группа ученых из Росси совместно с коллегами из
Финляндии и Германии сообщила в июньском номере журнала «ACS Omega» о значительном усилении
эффекта локального разрушения раковых
клеток, вызванного гипертермией радиочастотного диапазона, в присутствии
структурированных низкотоксичных пористых кремниевых нано нитей.
«Известно, что частицы нано размеров (до 100-200 нм)
при движении по кровеносным сосудам накапливаются в опухолях. Для их
использования в лечебных целях необходимо, что бы они достаточно интенсивно
поглощали электромагнитное излучение. В данной работе показано, что нано нити
структурированного кремния принципиально обладают рядом преимуществ достаточных
для использования их при лечении онкологических болезней с помощью
электромагнитного излучения» - сообщил соавтор статьи, кандидат
физико-математических наук, ведущий
научный сотрудник Лаборатории цитотехнологии и Лаборатории тканевой инженерии
Института Теоретической и Экспериментальной Биофизики РАН Андрей Александрович
Кудрявцев.
По словам Андрея Александровича в исследовании показано, что при контакте с
биологическими тканями происходит быстрая (24 часа) деградация этих частиц.
Этот эффект, достаточен для удаления наночастиц из организма после их
использования. В процессе деградации в области расположения наночастиц (в
опухоли) накапливаются ионы H+ и H3SiO4-.
В результате в этих областях увеличивается скорость поглощения электромагнитных
волн, увеличивается температура нагрева ткани, что и может вызвать
гипертермическую гибель клеток. Увеличение температуры ткани и, следовательно,
гибель клеток должна иметь место только в областях расположения наночастиц, то
есть в опухолях. Известно, что области с повышенным содержанием ионов
интенсивно поглощают рентгеновское излучение. Этот эффект позволяет в процессе
лечения контролировать накопление наночастиц в опухоли и последующую ремиссию
опухоли по яркости рентгеновского
изображения исследуемого органа или ткани.
Работа
поддержана грантом РНФ (17-72-10200) и по программе «УМНИК» Фонд содействия
развитию малых форм предприятий в Науке и технике (13098GU /2018).
Источники:
M.
Gongalsky,
G.
Gvindzhiliia,
K.
Tamarov,
O.
Shalygina,
A.
Pavlikov,
V.
Solovyev,
A.
Kudryavtsev,
V.
Sivakov
and
L.
Osminkina.
Radiofrequency hyperthermia
of cancer cells enhanced by silicic acid ions released during the
biodegradation of porous silicon nanowires. ACS Omega 2019, 4, 10662−10669
https://pubs.acs.org/doi/full/10.1021/acsomega.9b01030
Материал подготовила:
Алсу Дюкина
Пресс-служба ИТЭБ РАН, iteb-press@yandex.ru,
Пресс-релизы ИТЭБ РАН: http://web.iteb.ru/press-release.htm
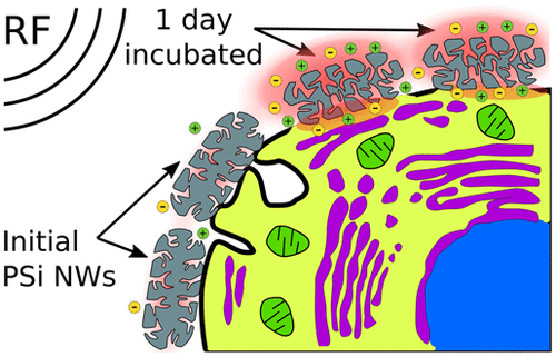
Рисунок.
Схематическое изображение механизма радиочастотной (RF) сенсибилизации пористых
кремниевых (PSi) нанонитей (NWs).
Красноватое свечение вблизи PSi
представляет
радиочастотный нагрев. Маленькие зеленые и желтые кружки - катионы и анионы
кремниевой кислоты соответственно. PSi NWs
слева
представляют собой исходные частицы с толстыми стенками кремния, а PSi NWs
в
области цитоплазматической мембраны (окрашены в черный цвет) представляют собой
частицы с высоким биоразложением с тонкими стенками кремния после 24 ч
инкубации. Разрушение мембраны в области «горячих» PSi NWs
показано
в виде разрывов черной линии.
На
фото соавтор статьи к.ф-м.н., в.н.с. ИТЭБ РАН Кудрявцев Андрей Александрович