http://93.174.130.82/digest/showdnews.aspx?id=0e1db16f-2dda-4fa6-9583-b8ae58167f71&print=1
© 2025 Российская академия наук
Мощный линейный ускоритель протонов, единственный такого типа на
евро-азиатском континенте, находится в Институте ядерных исследований
Российской академии наук в Троицке, в 20 километрах к югу от МКАД. Он «питает»
комплекс установок для фундаментальных и медицинских исследований. Корреспондент
Naked Science побывал там и поговорил с учеными об их достижениях, текущих
экспериментах, а также о том, что мешает им использовать возможности ускорителя
по максимуму.
Территория у Института ядерных исследований огромная. За плотным
заснеженным лесом даже не видно зданий. Мы высаживаемся из автобуса у бетонной
коробки, в которой на первый взгляд нет ни одного окна. Заходим через тяжелые
двери; внутри, как и снаружи, все выглядит не слишком современным, как будто
машина времени перекинула нас этак на полвека назад, в советское прошлое. Так
мы оказываемся в одном из зданий Ускорительного комплекса Института ядерных
исследований Российской академии наук (ИЯИ РАН).
Спускаемся. Краска на стенах давно потрескалась. На входе в туннель под
железными плитами привольно растеклась большая лужа; как нам объясняют, недавно
прорвало коммуникации. Впрочем, эти мелочи отходят на второй план, как только
мы видим сам ускоритель: даже спустя десятилетия после своей постройки он выглядит
впечатляюще. Обвитая проводами труба выходит из стены в десятках метрах слева и
тянется направо, насколько хватает взгляда. Мы стоим в самом ее начале.
Всё в резонансе
Слева за стеной находятся два источника частиц, подающих поток
положительных ионов водорода с энергией около 400 килоэлектронвольт, которому
предстоит разогнаться в тысячу раз. Делается это с помощью резонансного
ускорения.
Его базовый принцип достаточно прост для понимания: внутри ускорителя
создаются электромагнитные волны. Оказавшись под действием таких волн, частица будет
то ускоряться, то замедляться, следуя меняющемуся направлению электрического
поля. Но что если на периоды замедления частицу как бы прятать от поля? Тогда
она будет исключительно ускоряться.

Внутренний вид резонаторов с
трубками дрейфа начальной части
Частицы «прячут» от поля с помощью так называемых трубок дрейфа. Вот
частица влетает в ускоритель, чуть-чуть ускоряется, но в тот момент, когда поле
начинает менять направление, она оказывается под защитой трубки, где дрейфует
некоторое время, соответствующее размеру трубки. А трубка заканчивается как раз
тогда, когда поле повернулось в сторону ускорения.
Вначале, когда энергия маленькая, трубки совсем небольшие, и это видно
по устройству ускорителя — они стоят буквой V, потому что длины волны не хватает,
чтобы поставить их друг за другом. Но постепенно они становятся все длиннее и
длиннее. На выходе из первого резонатора пучок с начальной энергией 400
килоэлектронвольт разгоняется до 20 МэВ.
Физический пуск этой первой части ускорителя состоялся в 1988 году.
Тогда пучок частиц тоже разогнали до энергии 20 МэВ. По мере усиления питания и
введения новых резонаторов — всего их пять — росла и энергия. В 1996 году
добились энергии 502 МэВ, но постепенно элементы (клистроны) начали выходить из
строя, энергия падала. Сегодня максимум ускорителя — 300 МэВ, и причины этого,
увы, чисто экономические.
Резонаторы — гигантские многослойные «бочки». Внутри они покрыты
рафинированной бескислородной медью для хорошей электропроводности. Снаружи — нержавеющая
сталь, защищающая от внешней среды. Посередине — слой углеродистой стали для
хорошей теплоотдачи, над которым проложены каналы водоохлаждения.
Общая длина ускорителя — около 720 метров, в конце — комплекс установок
для теоретических и практических исследований, а также центр протонной терапии.
А на отметке около 200 метров есть ответвление — пучок отводят на производство
радиоизотопов.
Полвека истории
История работы с изотопами началась в конце 1980-х, когда ускоритель
еще только строили. «Когда энергия достигла уровня 160 МэВ, появилась
возможность использовать пучок протонов для наработки различных изотопов,
в основном медицинского назначения», — рассказывает Борис Леонидович Жуйков,
доктор химических наук, заведующий радиоизотопным комплексом в ИЯИ РАН.
Параметры ускорителя позволяли получать изотопы, которые невозможно
получать на других ускорителях (а если и возможно — то в небольших
количествах). «Отличие в том, что наш ускоритель обеспечивает одновременно и
достаточно высокую энергию протонов, что приводит к образованию радионуклидов с
большим числом нейтронов, вылетающих из ядра, и высокую интенсивность, что
позволяет производить изотопы в большом количестве», — продолжает Борис Леонидович.
Когда в 1992 году состоялся запуск, это была самая мощная в мире установка
для генерации изотопов, которые вообще можно получать на ускорителях.

Борис Леонидович Жуйков, доктор
химических наук, заведующий радиоизотопным комплексом в ИЯИ РАН
Ставку сделали на стронций-82, который применяли в еще только
развивавшемся тогда методе позитронной томографии. Многие не верили в его
перспективность, но надежды оправдались. Метод становился все более популярным,
и спрос на стронций-82 в мире увеличивался.
Ученые ИЯИ РАН начали сотрудничать сначала с Канадой и США, а позже с Францией.
«Все понимали, что невыгодно производить только то небольшое количество
изотопов, в котором нуждалась наша страна. Мы стали развивать высокопроизводительные
методы, а это означало сотрудничество со странами, где ядерная медицина была
развита гораздо больше, чем в России, — объясняет Борис Леонидович. — Наиболее
плодотворной оказалась работа с американскими коллегами. В середине 1990-х они
выделили большие средства на наши исследования».
В результате была разработана и налажена вся технологическая цепочка
производства: наработка на ускорителе большого количества стронция-82 из
металлического рубидия, химическое выделения стронция-82 (вторая стадия) и
изготовление генератора рубидия-82 (третья стадия), который используют медики.
Далее коллеги из РНЦРХТ им. А. М. Гранов (Санкт-Петербург) с участием ученых
ИЯИ РАН провели полный цикл клинических испытаний по применению этого
радионуклида для диагностики кардиологических и онкологических заболеваний.

Медицинский генератор стронций/рубидий-82. В нем радионуклид
стронций-82 (период полураспада 25,3 дня), который нарабатывают на ускорителе
ИЯИ РАН, распадается с образованием рубидия-82 (период полураспада 75 с),
применяемого в медицинской диагностике / «Вот так, в буквальном смысле слова с
нуля. Когда мы начали, тут было просто болото. Мы построили установку на пучке
ускорителя, разработали весь процесс начиная с ядерно-физических и химических
исследований и завершая диагностикой пациентов, — подытоживает Борис
Леонидович. — По примерным подсчетам, с помощью изотопов, произведенных на
нашей установке, было продиагностировано и, будем надеяться, вылечено около 350
тысяч пациентов. А если учесть наши технологии, внедренные в России, США,
Франции, Канаде и Южной Африке, то счет пойдет на миллионы».
Планы на будущее
После 2014 года международное сотрудничество резко сократилось. Именно
за счет такого сотрудничества в большой степени развивались и финансировались
радиоизотопные исследования. Сегодня ИЯИ РАН ведет переговоры с крупным
бизнесом и ждет поддержки государства. И продолжают расширять возможности
получения медицинских изотопов.
В планах — регулярно получать разные изотопы не только для диагностики,
но и для терапии. По словам Жуйкова, самый перспективный изотоп, который на
этом ускорителе можно получать в больших количествах, — актиний-255. Этот радионуклид
испускает альфа-частицы, тяжелые и с большой энергией, но действующие только на
очень малых расстояниях и убийственные для раковых клеток.
В радионуклидных фармацевтических лекарственных препаратах (РФЛП) используют
известные биологически активные соединения, к которым вместо каких-то частей
молекул крепят радионуклиды. Известно, как эти соединения распределяются и
накапливаются в организме. Оказалось, что некоторые из них достигают максимальной
концентрации в опухолях. Поэтому с помощью таргетной терапии можно доставлять
актиний-255 напрямую к раковым клеткам и их уничтожать. Такой подход еще только
развивается, но уже показывает высокую эффективность.
На ускорителе в Троицке можно получать рекордное в мире количество
изотопа актиний-255 и поставлять его как российским, так и зарубежным
медицинским организациям, что способствовало бы развитию отечественной ядерной
медицины. «Наше государство не дает достаточно денег на эти исследования, и мы
ранее развивались в основном за счет коллабораций с иностранными партнерами», —
с сожалением завершает свое выступление Борис Леонидович.

Чем дальше, тем сильнее сужается
ускоритель. На снимке фрагмент ускорителя недалеко от отвода пучка в изотопный
комплект
У отечественной ядерной медицины долгая история. Она развивалась в ногу
с атомными технологиями. К середине XX века в стране появилось уже несколько
производств изотопов. Сегодня ядерная медицина вышла на новый виток развития, и
опытные специалисты с настолько мощной установкой могут сыграть в нем важную
роль.
Сам комплекс получения изотопов нам не показали, потому что он на
реконструкции. И чтобы попасть к установкам в конце ускорителя, мы вышли на
улицу. Под хруст снега под ногами и рассказ про историю развития комплекса мы
больше десяти минут шли вдоль покрытого холмом туннеля ускорителя.
Ускоритель создавали под проект Московской мезонной фабрики на основе
сильноточного линейного ускорителя протонов и отрицательных ионов водорода на
энергию 600 МэВ. Сегодня физика мезонов уже не актуальна, свою первичную
научную программу ускоритель выполнил. Но появились новые задачи — как
фундаментальные, так и прикладные. Через несколько десятилетий работы установок
класса «мегасаенс» обычно проводят капитальный ремонт, а сам ускоритель
модернизируют под новую научную программу: меняют интенсивность пучка, строят
дополнительные каналы вывода, настраивают новые режимы работы.
«Поскольку нерационально разбирать или даже просто останавливать
установку, мы ищем другие методы исследования и потребителей нынешних
возможностей ускорителя. Без модернизации принципиально новые параметры мы не
получим, но можно их немного улучшить и создать новые исследовательские стенды.
С этим можно и нужно работать», — комментирует Сергей Александрович Гаврилов,
заведующий лабораторией пучка отдела ускорительного комплекса ИЯИ РАН.

Сложенный из больших бетонных блоков «саркофаг» — защита от излучения
Заходим в здание, проходим в неприметную дверь, и потолок «улетает»
ввысь. Мы оказываемся в огромном гулком строении вроде самолетного ангара со
сложенными из больших бетонных блоков «саркофагом», покрывающим почти всю
территорию. Блоки — биологическая защита от ионизирующего излучения. В толще
блоков на глубине четырех метров оборудованы хранилища для промежуточного
хранения отработанных радиоактивных корпусов нейтронных источников и ловушек
пучка, а также корпусов установок, отработанных фильтров и модулей нейтронного
источника.
Здесь ускоритель заканчивается, разветвляясь на несколько стендов:
комплекс импульсных источников нейтронов, светосильный спектрометр по времени
замедления нейтронов и комплекс протонной терапии.
Поднимаемся на бетонные блоки. В нескольких метрах под ногами — канал,
по которому протоны летят к вольфрамовой мишени и выбивают потоки нейтронов. Благодаря
своей нейтральности эти частицы относительно свободно проникают в межатомные
области и взаимодействуют с ядрами. Поэтому по рассеянию нейтронов можно
изучать пространственное строение вещества и получать бесценные знания о
конденсированных средах, а также о химических, биологических и других веществах.
У этого ускорителя, конечно, не только прикладное значение. Он немало
принес фундаментальной науке: было проведено большое количество исследований
трансурановых элементов, опасных отходов ядерной энергетики. Сейчас эти изотопы
просто захоранивают, но теоретически они могут быть источником энергии, важным
элементом замкнутого ядерного топливного цикла.
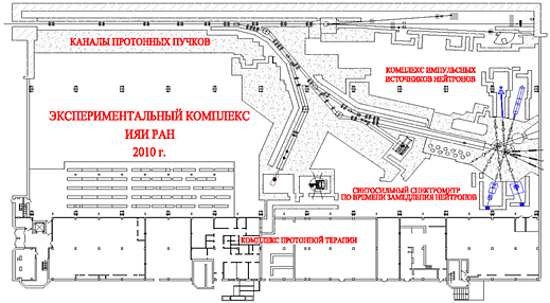
Схема экспериментального комплекса
линейного ускорителя ионов водорода ИЯИ РАН
А одно из основных направлений — материаловедение. На установке
диагностируют новые материалы, проверяют, соответствуют ли их свойства тем,
которые которые хотели получить создатели. В некоторых случаях, если требуется,
удается пронаблюдать процесс плавления. В частности, тестируют стали и сплавы,
которые используются в ядерной физике для защиты ядерных реакторов. И наблюдают
влияние заряженных частиц на материалы микроэлектроники для космоса.
На вопрос, получается ли по результатам сделать материал с заданными
свойствами, Равиль Асхатович Садыков, ведущий научный сотрудник ИЯИ РАН,
отвечает: «Дай бог! Это нешуточное дело. Иногда требуется очень много опытов,
чтобы получить то, что хочешь, иначе мы с вами давно бы ходили в других вещах.
Были бы одеты и обуты [в материалы с любыми задуманными и заданными
характеристиками]».
И, хочется добавить, вылечили бы рак. Именно такие технологии
тестируются сегодня в комплексе протонной терапии.
В погоне за раковыми клетками
Если изотопы нужны для диагностики и лечения рака изнутри организма, то
протонная терапия — это внешнее воздействие. При традиционной лучевой терапии
умирают как больные, так и здоровые клетки, поэтому ее нельзя использовать,
когда опухоль находится рядом с жизненно важными органами: мочевым пузырем, сердцем,
некоторыми участками мозга.
Протоны отличаются от других частиц тем, что выделяют максимальную дозу
не на поверхности тела, а на заданной глубине, то есть могут пролетать сквозь
ткани до опухоли с незначительным повреждением нормальных тканей. «Об этом
преимуществе протонов известно с середины прошлого века», — объясняет Сергей
Всеволодович Акулиничев, доктор физико-математических наук, заведующий
лаборатории медицинской физики ИЯИ РАН.
Традиционную лучевую терапию в больницах по всему миру проводят в
несколько сеансов, облучая нужное место в организме на протяжении длительного
времени, но с низкой интенсивностью. Причина в том, что здоровые клетки тоже
страдают от радиации, и низкая интенсивность позволяет смягчить побочные
эффекты. Именно поэтому врачи боялись ее наращивать, несмотря на то, что
лабораторные эксперименты с клетками и животными показывали, что если ту же
дозу радиации давать быстрее, за доли секунды, то здоровые клетки страдают
значительно меньше, чем раковые.
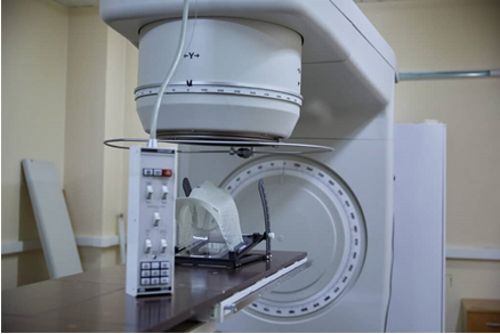
Установка фотонной радиотерапии в
комплексе протонной терапии
Переломный момент произошел несколько лет назад. Обычная
терапия вызывала у пожилого пациента с Т-клеточной лимфомой кожи слишком
сильную реакцию здоровых тканей, и его врачи попробовали использовать
флеш-метод. Пациент вылечился. Вскоре после этого врачи во Франции успешно
опробовали флеш-метод в протонной терапии. В прошлом
году завершилось первое клиническое испытание протонной флеш-терапии
для лечения пациентов с метастазами в костях. В декабре прошла уже вторая
международная конференция, посвященная флеш-терапии. Эффективность метода
общепризнана.
«Нам казалось, что у нашего ускорителя интенсивность пучка слишком
большая, и мы искусственно ее занижали. Но потом мы провели опыты, протестировали
разные резжимы. Обнаружили, что наш ультрафлеш режим, недоступный другим
ускорителям, вызывает еще более сильный апоптоз в опухолевых клетках по
сравнению с нормальными», — рассказывает Сергей Всеволодович. Если в
международно признанном флеш-режиме доза излучения подводится за полсекунды, то
в ультрафлеш-режиме — за 100 микросекунд.
Разницу в реакции клеток оценивают по фактору сохранения (sparing
factor), равному соотношению уровня повреждения опухолевых клеток к уровню
повреждения нормальных. Критерием могут быть разные показатели, от апоптоза
(генетически запрограммированной «аккуратной» смерти клеток) до экспрессии
генов.

Сергей Всеволодович Акулиничев,
доктор физико-математических наук, заведующий лаборатории медицинской физики
ИЯИ РАН
По словам Сергея Всеволодовича, вскоре они перейдут от опытов с
клетками к первым опытам с живыми организмами. Затем начнут эксперименты с
животными с подсаженными опухолевыми клетками. Пока по показателям апоптоза
фактор сохранения в режиме ультрафлеш выше, чем при флеш-терапии. Для
публикации в международном научном журнале потребуется проверить и другие
показатели.
На вопрос Naked Science о том, можно ли как-то ускорить эти
исследования, Сергей Всеволодович качает головой: «Бюрократических препон здесь
нет. Просто нужно пройти все этапы. Мы много раз докладывали о наших
результатах, но для убедительной публикации нужно больше статистики. Ведь мы
претендуем на серьезное открытие».
Для медицинских целей не строят настолько мощные ускорители протонов,
поэтому возможность вести такие исследования есть у немногих. В России
результаты можно будет подтвердить еще как минимум на одной установке —
«Циклотроне-80» в Гатчине. «У них тоже была проблема чрезвычайной интенсивности
пучка, который они собирались занижать для лучевой терапии. Мы можем
порекомендовать им не терять в интенсивности, а сократить время воздействия на
мишень», — добавляет Сергей Всеволодович.
«Если мы подтвердим биологические преимущества нашего метода, то на
будущих ускорителях можно будет закладывать такую мощность в конструкцию на
этапе проектирования. Фактически, мы нарабатываем знания для новых
ускорителей», — подытоживает ученый.
При таком количестве опытов и направлений исследований возникает
вопрос, справится ли установка, если спрос вырастет. «Сеанс — это
круглосуточная работа. Такая машина не может включаться и выключаться по
запросу. Запускается весь комплекс зданий, и люди работают в две смены, —
отвечает на вопрос Naked Science Сергей Александрович Гаврилов,
заведующий лабораторией пучка отдела ускорительного комплекса ИЯИ РАН. — Как
правило, длительность работы зависит от потребителя. Стандартный сеанс на
изотопы длился две недели. Процедура проверки радиационной стойкости материалов
— более быстрая. Один ускорительный „выстрел” — и микросхема получила
повреждения, еще несколько — и она умерла, готовят следующую. Такие сеансы
длятся несколько дней. Длинных сеансов по две-три недели у нас от трех до пяти
в год. Короткие по потребности».
Установка может работать в круглосуточном режиме, но сейчас для
беспрерывного круглосуточного дежурства не хватает людей. Сергей Александрович
уверен, стоит институту объявить о готовности установки работать больше, и
потребители пучка найдутся.
Ускорительный ренессанс
Ускорителю необходимы капитальный ремонт и модернизация. «У нас уже
есть инфраструктура. Не нужно ломать ее и строить что-то принципиально новое.
Нет людей, готовых это делать. Это дорого и долго, займет не один десяток лет.
Лет пять нужно разрабатывать технический проект, потом вдвое больше изготавливать
комплектующие и строить новую установку. Через 20 лет он, наконец, будет
запущен, но уже с устаревшими запланированными характеристиками. Давайте
улучшим характеристики существующей машины в несколько раз. Поднимем энергию и
ток. Позовем новых пользователей!»

Сергей Александрович Гаврилов,
научный сотрудник отдела ускорительного комплекса ИЯИ РАН
По словам Сергея Александровича, на этом ускорителе первичную
эффективную модернизацию можно провести всего за два-три года. Для начала нужно
обновить источники питания системы фокусировки и систему синхронизации,
модернизировать линии питания дополнительных резонаторов для поднятия энергии.
Следующий шаг — переход на частоту следования импульсов пучка 100 Герц (сейчас
— 50 герц) для увеличения средней интенсивности пучка.
«В стране начался ускорительный ренессанс, — смеется Сергей
Александрович. — Выделены деньги на федеральную научно-техническую программу
синхротронных и нейтронных исследований. Мы в ней активно участвуем, но наш
ускоритель в нее не попал. Хотели его улучшить, но ускорительная часть
программы нацелена на строительство новых комплексов на основе циклических
машин, а также компактных линейных ускорителей для небольших исследовательских
центров и учебных заведений».
Создается впечатление, что все научные группы, работающие с установкой
класса «мегасаенс», полностью уверены в ее уникальных возможностях: от
фундаментальных исследований до наработки медицинских изотопов и противораковой
ультра-флеш терапии. И за время поездки сумели заразить этой уверенностью
участников экскурсии. Мы выходим из бетонной коробки на морозный воздух с
надеждой, что для установки найдется финансирование.